คำตอบของทีม
ไม่ได้ส่งคำตอบ
ไม่ได้ส่งคำตอบ
คะแนน + โบนัสทำเร็ว
0.0
0.0
ไม่ได้ส่งคำตอบ 
เมื่อนำน้ำจากบ่อบาดาลในจังหวัดกาญจนบุรีมาทดสอบหาความกระด้าง (Ca2+ และ Mg2+) ด้วยเทคนิคทาง atomic absorption spectrophotometry พบว่าในตัวอย่างมีปริมาณ Ca2+ และ Mg2+ เท่ากับ 0.03 และ 0.02 mol/L ตามลำดับ หากเราต้องการแยก Ca2+ ออกจาก Mg2+ ด้วยการตกตะกอนกับ fluoride (F–)
คำถาม
$\quad$1. เราจะต้องใช้ fluoride อย่างน้อยที่สุดที่ความเข้มข้นเท่าใด (ในหน่วย $\times$10–5 mol/L) ที่จะทำให้ Ca2+ ตกตะกอน
$\quad$2. เราจะต้องใช้ fluoride อย่างน้อยที่สุดที่ความเข้มข้นเท่าใด (ในหน่วย $\times$10–5 mol/L) ที่จะเริ่มทำให้ Mg2+ ตกตะกอน
ข้อมูล Ksp CaF2 = 1.2$\times$10–11, Ksp MgF2 = 8.0$\times$10–8
คำแนะนำสำหรับการตอบคำถามแบบตัวเลข
• ให้ตอบคำตอบตัวเลขเป็นจำนวนเต็มแบบไม่ต้องใส่เลขทศนิยม โดยหากตัวเลขที่คำนวนได้มีเลขทศนิยมให้ปัดเศษของทศนิยมทิ้งเสมอ
• โจทย์ข้อนี้ต้องตอบตัวเลข 2 คำตอบ สำหรับข้อ 1 และ 2 ตามลำดับ
• ในกรอกคำตอบลงในช่องว่าง กำหนดให้คำตอบตัวเลขแรกสำหรับคำตอบในข้อที่ 1 และคั่นด้วยเครื่องหมาย ; และใส่คำตอบในข้อที่ 2 (โดยไม่ต้องเว้นวรรค)
ตัวอย่างเช่น คำตอบที่คำนวนได้จากโจทย์ข้อที่ 1 และ 2 คือ 5.2$\times$10–5 mol/L และ 73.7$\times$10–5 mol/L ตามลำดับ แล้ว คำตอบที่กรอกต้องกรอกลงไปคือ 5;73
คำถาม
$\quad$1. เราจะต้องใช้ fluoride อย่างน้อยที่สุดที่ความเข้มข้นเท่าใด (ในหน่วย $\times$10–5 mol/L) ที่จะทำให้ Ca2+ ตกตะกอน
$\quad$2. เราจะต้องใช้ fluoride อย่างน้อยที่สุดที่ความเข้มข้นเท่าใด (ในหน่วย $\times$10–5 mol/L) ที่จะเริ่มทำให้ Mg2+ ตกตะกอน
ข้อมูล Ksp CaF2 = 1.2$\times$10–11, Ksp MgF2 = 8.0$\times$10–8
คำแนะนำสำหรับการตอบคำถามแบบตัวเลข
• ให้ตอบคำตอบตัวเลขเป็นจำนวนเต็มแบบไม่ต้องใส่เลขทศนิยม โดยหากตัวเลขที่คำนวนได้มีเลขทศนิยมให้ปัดเศษของทศนิยมทิ้งเสมอ
• โจทย์ข้อนี้ต้องตอบตัวเลข 2 คำตอบ สำหรับข้อ 1 และ 2 ตามลำดับ
• ในกรอกคำตอบลงในช่องว่าง กำหนดให้คำตอบตัวเลขแรกสำหรับคำตอบในข้อที่ 1 และคั่นด้วยเครื่องหมาย ; และใส่คำตอบในข้อที่ 2 (โดยไม่ต้องเว้นวรรค)
ตัวอย่างเช่น คำตอบที่คำนวนได้จากโจทย์ข้อที่ 1 และ 2 คือ 5.2$\times$10–5 mol/L และ 73.7$\times$10–5 mol/L ตามลำดับ แล้ว คำตอบที่กรอกต้องกรอกลงไปคือ 5;73
เฉลย
ตอบ 2;200
แนวคิด
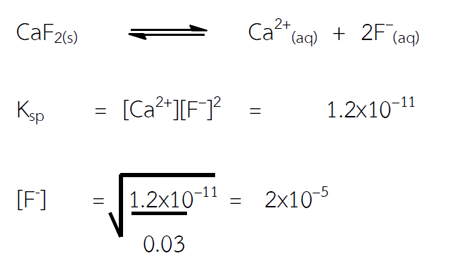
ความเข้มข้นของ F– ที่ต่ำที่สุดที่จะทำให้ Ca2+ ตกตะกอน = 2x10–5 mol/L
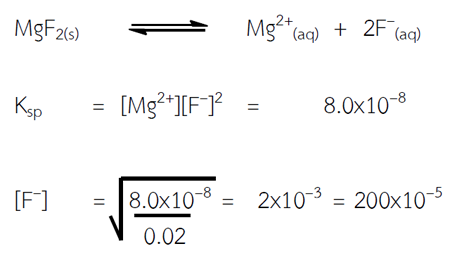
ความเข้มข้นของ F– ที่ต่ำที่สุดที่จะทำให้ Mg2+ ตกตะกอน = 200x10–5 mol/L